エネルギーデバイス班
現在、リチウムイオン二次電池(LIB)は、携帯電話や小型電子端末の電源として幅広く使用されています。近年では、電気自動車やドローンの需要が高まり、エネルギー密度について現行のLIBを上回る性能を発揮する次世代二次電池の開発が求められています。そこで、当研究室では、LIBへのリチウム金属負極や硫黄正極の適用や、新たなキャリアを使用した二次電池に関する研究を行っています。
バイオセンシング班
疾患の早期発見やヘルスケアデータ取得への貢献を目的に、生体関連分子の定量的な検出に向けた電気化学センサの開発を行っています。電気化学センサとは、分子の吸着、酸化還元反応、酵素反応などを認識し、電気的信号に変換するデバイスです。当研究室は電気化学センサの中でも、電界効果トランジスタ(Field-effect transistor: FET)バイオセンサ、アンペロメトリックセンサに関する研究を行っています。
エネルギーデバイス班
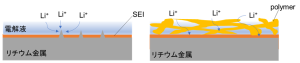
図1 (a) リチウム金属負極表面 (b)ポリマー膜適用時のリチウム金属負極表面
また、リチウムデンドライトの形成機構を解明することは、電池劣化状態の診断やリチウム金属負極界面の設計に繋がります。しかし、反応性の高いリチウム金属負極の動作機構の解析は、動作後の電池を分解した分析や,実際の動作系とは異なる特殊なセルが必要となる測定が主流となっています。そこで当研究室では交流インピーダンス法を用いた実用セルでの充放電試験中の動作解析も行っています。微小の交流信号を実用セルに印加し,各周波数におけるインピーダンスを分析する手法です。交流信号を用いることで、充放電反応を素過程に分離することが可能となるためリチウム金属負極の状態を非破壊で分析することを目指しています。加えて、リチウムデンドライトの成長過程のシミュレーションも行っています。温度や圧力、初期のリチウム金属表面の形状などの物理学的パラメータを変更して、デンドライトの成長課程をシミュレーションすることが可能であるため、リチウムのデンドライト成長に影響を与えるパラメータの判別に繋がり、リチウム金属負極のデンドライト形成対策の指針を得ることが期待されます。 さらに、新たなリチウムイオン電池の負極材料の設計も検討しています。リチウムとの合金化反応で容量を示す層状化合物は、充放電を繰り返すごとに、隣接する層と合体することで粒径が大きくなり、容量が低下することが懸念されます。そこで、合金化反応をする層状化合物の層間に非反応層を挿入することでサイクル経過後も層状構造を維持し、サイクル特性を向上させることを目指しています。また、非反応層の電気化学的な物性にも着目し、レート特性の向上のために電子伝導パスを確保することなども検討しています。- 参考文献
- D. Lin, Y. Liu and Y. Cui, “Reviving the lithium metal anode for high-energy batteries”, J. Nature Nanotech., 2017, 12, 194-206.
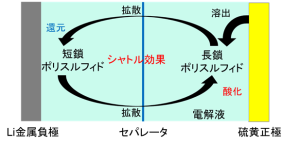
図1 シャトル効果の模式図
まず、リチウムポリスルフィドの溶出を防ぐ手法として、正極表面を負に帯電したポリマーでコーティングするという検討がなされていました(図2(a))[1]。このコーティングによりポリスルフィドアニオン(Sn2-)が静電反発により正極上に留まります。その結果,コーティングなしの場合(図2(b))と比較して,架橋ポリマーコーティングを施した場合(図2(d))は過充電が抑制されました。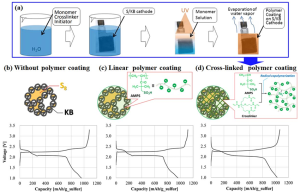
図2 (a)正極ポリマーコーティングの概要 (b)-(d)正極の模式図と充放電曲線
(b)コーティングなし (c)線状ポリマーコーティング (d)架橋ポリマーコーティング[1]
次に、過電圧を抑制する手法として,電解液へのレドックスメディエーター(RM)の導入が検討されています。通常の充電過程では絶縁性のLi2Sが正極表面上のみで電気化学的に酸化されるため,充電過電圧が大きくなります。一方RMを導入することで、RMが電気化学的に酸化された後にLi2Sを化学的に酸化するという機構に変化し、充電過電圧が抑制されます。現在当研究室では新規RMの探索を行っています。- 参考文献
- N. Nakamura, H. Mikuriya, E. Kojima, S. Ahn, K. Yamabuki, T. Momma, and T. Osaka, “Communication—Cross-Linked Anionic Polymer Coating Prepared by UV and Thermal Curing for Long-Life Lithium-Sulfur Battery”, J. Electrochem. Soc., 2021, 168, 110552.
バイオセンシングデバイス
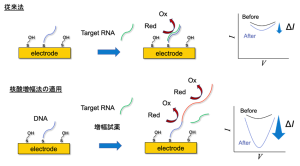
FETバイオセンサとは、荷電した標的分子の吸着によるゲート絶縁膜表面の電位変化を電界効果によるキャリア濃度の変化として検出するセンサです。半導体加工技術による通信回路等との集積化や、マルチチャネル化による複数の対象の同時測定、小型化が期待されます[1]。また、大量生産によるコストダウンも見込まれます[1]。当研究室はこれまで、 FETバイオセンサを用いた生体分子検出に取り組んできました。具体的には、抗体あるいは抗原結合性フラグメントをプローブとした腫瘍マーカーの検出や抗原を固定化した系での免疫グロブリンEの高感度検出、アルツハイマー病の早期発見に向けたコンゴーレッド固定化FET によるアミロイドβの検出、糖鎖固定化FET によるインフルエンザウイルスの検出などが挙げられます[2][3][4][5][6]。最近では、等温核酸増幅法を利用したRNAの高感度検出や、競合法を利用した抗がん剤5-Fluorouracilの検出を実現しました[7][8]。現在は、ストレスホルモンとして知られるコルチゾールの高感度検出や、センサ応答の再現性向上に向けた測定システムの構築に取り組んでいます。
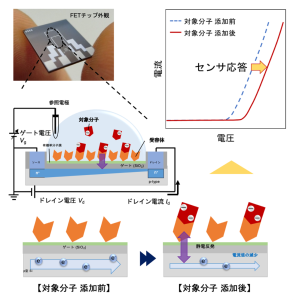
図1 FETバイオセンサの検出概要図
- 参考文献
- 黒岩繁樹, 大橋啓之, 逢坂哲彌, "4. 電界効果トランジスタを用いたイオセンサの展開", 電気化学, 2020, 88, 317-325.
- S. Hideshima, R. Sato, S. Kuroiwa and T. Osaka, "Fabrication of stable antibody-modified field effect transistors using electrical activation of Schiff base cross-linkages for tumor marker detection", Biosens. Bioelectron., 2011, 26, 2419-2425.
- S. Hideshima, M. Kobayashi, T. Wada, S. Kuroiwa, T. Nakanishi, N. Sawamura, T. Asahi, T. Osaka, "A Label-Free Electrical Assay of Fibrous Amyloid β Based on Semiconductor Biosensing", Chem. Commun., 2014, 50, 3476-3479.
- S. Cheng, K. Hotani, S. Hideshima, S. Kuroiwa, T. Nakanishi, M. Hashimoto, Y. Mori, T. Osaka, "Field effect transistor biosensor using antigen binding fragment for detecting tumor marker in human serum", Materials, 2014, 7, 2490-2500.
- S. Hideshima, H. Hayashi, H. Hinou, S. Nambuya, S. Kuroiwa, T. Nakanishi, T. Momma, S.Nishimura, Y. Sakoda and T. Osaka, "Glycan-immobilized dual-channel field effect transistor biosensor for the rapid identification of pandemic influenza viral particles”, Sci. Rep.,2019, 9, 11616.
- S. Hideshima, S. Kuroiwa, M. Kimura, S. Cheng, T. Osaka, " Effect of the size of receptor in allergy detection using field effect transistor biosensor", Electrochimica Acta,2013, 110, 146-151.
- H. Hayashi, M. Fujita, S. Kuroiwa, K. Ohashi, M. Okada, F. Shibasaki, T. Osaka, T. Momma, “Semiconductor-based biosensor exploiting competitive adsorption with charged pseudo-target molecules for monitoring 5-fluorouracil concentration in human serum”, Sens. Actuators, 2023, 395,134495.
- H. Hayashi, A. Enami, H. Fujita, S. Kuroiwa, K. Ohashi, M. Kuwahara, T. Osaka, T. Momma, ”Field-effect transistor biosensor with signal amplification by ternary initiation complexes for detection of wide-range RNA concentration”, Talanta, 2024, 273, 125846.